1- ¿Qué son los isómeros?
Los isómeros son compuestos orgánicos que tienen fórmulas moleculares idénticas, pero que se diferencian en la naturaleza o el orden de los enlaces entre sus átomos o en la disposición de sus átomos en el espacio.
Pueden clasificarse como isómeros constitucionales y como estereoisómeros:
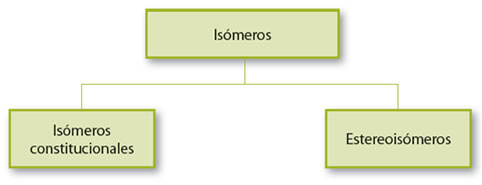
Los isómeros constitucionales, son aquellos en donde las moléculas poseen la misma fórmula molecular, pero tienen una diferente distribución de los enlaces, entre sus átomos, lo que se traduce en diferentes formas estructurales.
Dentro de los isómeros constitucionales se encuentran los isómeros de cadena, los isómeros de posición y los isómeros de función.
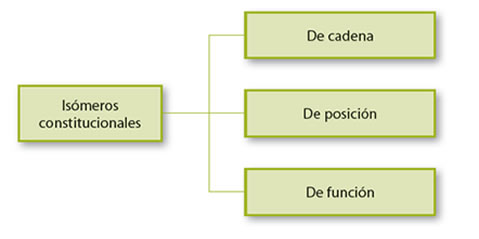
Los isómeros de cadena, corresponden a isómeros que tienen los componentes de la cadena hidrocarbonada acomodados en diferentes lugares, es decir, las cadenas que poseen, son diferentes, ya que presentan distinto esqueleto o estructura. Por ejemplo, el pentano (C5H12), presenta varios isómeros, pero los más conocidos son el isopentano y el neopentano:
pentane
(n-pentane)
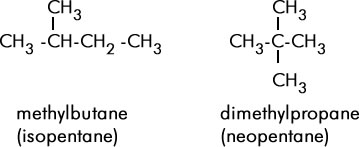
En este caso, las cadenas de carbono cambian según el compuesto, sin embargo, la fórmula estructural de todos ellos, es la misma (C5H12)
Los isómeros de posición, corresponden a compuestos que presentan el mismo grupo funcional, pero sin embargo, éste se encuentra en distintas posiciones de la cadena carbonada. Corresponden a isómeros de posición el 2-hexanol y el 3-hexanol, cuya fórmula molecular es (C6H14O)

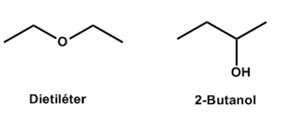
Los isómeros de función corresponden a compuestos orgánicos que difieren en el grupo funcional que presentan en su estructura. Son ejemplos de isómeros de función el dietil éter y el 2-butanol, compuestos que presentan como fórmula C4H10O.
Por otro lado, los estereoisómeros corresponden a compuestos que están formados por el mismo tipo y número de átomos unidos en la misma secuencia, pero que varían en la disposición espacial de estos.
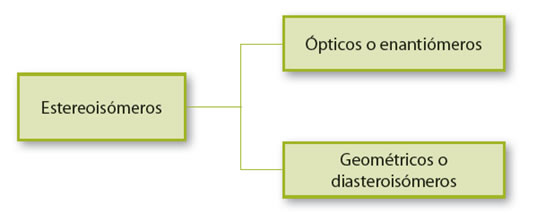
Hay dos tipos de estereoisómeros, los isómeros ópticos o enantiómeros y los isómeros geométricos o diasteroisómeros:
Los isómeros ópticos o enantiómeros corresponden a moléculas que guardan entre sí una imagen especular, sin embargo, no se pueden superponer mutuamente. Esto significa que no es posible lograr que ambas moléculas calcen o coincidan una sobre la otra.
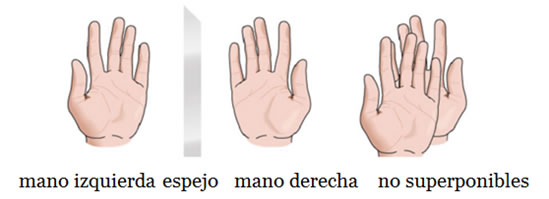
Los isómeros ópticos se denominan quirales, ya que, este término se relaciona con las manos, que al igual que estas moléculas son especulares entre sí, pues, son imágenes reflejadas en un espejo, sin embargo, si se tratan de hacer coincidir ambas manos, no se logra, porque no son superponibles.
Un carbono quiral, será aquel que está unido a diferentes grupos de átomo. También recibe el nombre de carbono estereogénico o estereocentro.

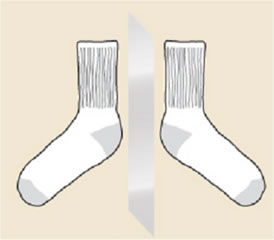
Aquellas moléculas que son imágenes especulares y que además son superponibles entre sí, se denominan aquilares. Son aquilares, por ejemplo, los calcetines, ya que se reflejan en un espejo, y además es posible hacerlos calzar entre sí.
Cuando una molécula presenta un plano de simetría corresponde a una molécula aquiral.
Los enantiómetros tienen propiedades físicas idénticas, tales como, el punto de ebullición y de fusión, la solubilidad, la densidad, la conductividad, entre otras.
Por ende, la única forma de diferenciarlos es a través de la actividad óptica, que las parejas de enantiómeros poseen.
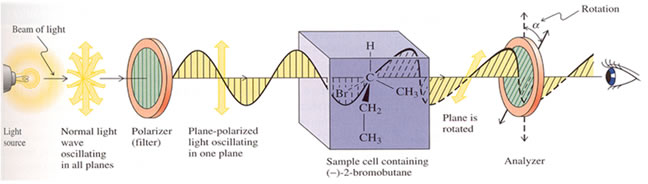
Cuando la sustancia no es ópticamente activa no hay cambios en el plano de vibración de la luz polarizada que se emite.
Si la sustancia si presenta actividad óptica, se observa una rotación en diferentes ángulos, según el plano de vibración de la luz polarizada que se emite.
Cuando la rotación del plano de la luz es hacia la derecha, en el sentido de las agujas del reloj, la sustancia es dextrógira (+). Si el giro es hacia la izquierda, en el sentido contrario a las agujas del reloj, la sustancia es levógira (-).
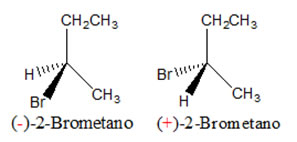
Como los enantiómeros son siempre dos, se debe utilizar algún método para poder diferenciarlos. Por lo general, cada uno de ellos, presentará la designación R o S.
Para determinar cuando un isómero será R o S, se deben utilizar las reglas de prioridad establecidas por Cahn, Ingold y Prelog.
Los pasos a seguir para poder determinar la designación son:
1. Se debe clasificar los sustituyentes del estereocentro según la prioridad. Para ello, se deben ordenar los cuatro grupos sustituyentes del carbono quiral por orden decreciente del número atómico de los átomos enlazados a él. Es decir, a mayor número atómico, mayor es la prioridad del sustituyente.
2. Si dos o más de estos átomos son iguales se recurre a considerar los átomos unidos a ellos con el mismo criterio de preferencia antes mencionado.
3. En el caso, que la ambigüedad persista, se recurre a considerar el tipo de enlace que une a los átomos en cuestión, dándolo preferencia al enlace triple, luego al enlace doble y finalmente, al enlace simple.
4. Finalmente, cuando se ha establecido el orden correcto de prioridad, se debe orientar la molécula en el espacio. El tetraedro correspondiente al carbono quiral se debe orientar de manera tal que el sustituyente con la menor prioridad se encuentre en el vértice más alejado del observador.
Si el orden de prioridad se hace en el sentido de las agujas del reloj, el carbono quiral recibe la denominación R, que significa rectus en latín.
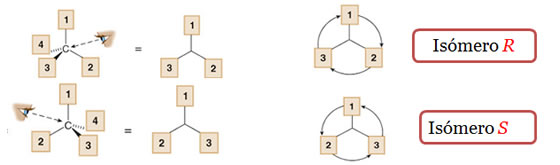
En el caso, que el orden de prioridad sea en el sentido contrario a las agujas del reloj, la denominación del carbono quiral es S, que significa sinister en latín.
Por ejemplo, la denominación que presentan los enantiómetros de la molécula 2-butanol, se representa a continuación:
– En primera instancia, se debe escribir la fórmula semidesarrollada del compuesto.
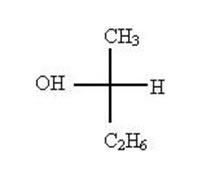
– Se debe asignar prioridad a los átomos correspondientes. Quién presenta la mayor prioridad es el OH, y quién menos, el H, por ende, el H debe estar lo más lejos del observador posible. El C2H6 es quién presenta la segunda prioridad y la tercera es el CH3.
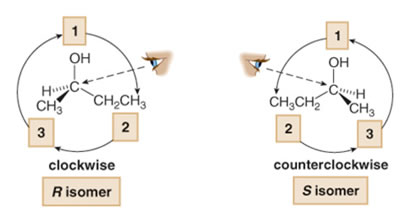
Por lo tanto, es posible encontrar el (R)-2-butanol, en donde, la rotación ocurre en el sentido de las agujas del reloj, y el (S)-2-butanol, donde la rotación ocurre en sentido contrario a las agujas del reloj.
Los isómeros geométricos o diasteroisómeros, corresponden a estéreoisómeros en los cuales hay presente un enlace doble, en los cuales, solo hay una diferencia en la disposición espacial de los átomos que lo forman.
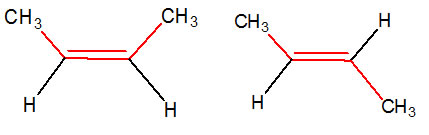
Cuando los átomos iguales del compuesto se encuentran en el mismo lado de la molécula, el isómero lleva el prefijo cis-, mientras que, si ambos átomos se encuentran en posiciones opuestas, el prefijo que se utiliza es trans-.

2- El uso de isómeros en ciertos medicamentos
Los isómeros ópticos también se conocen como enantiómeros. Estos son imágenes especulares, por lo que, no se puede superponer una a la otra.
Los enantiómeros fueron descubiertos por Louis Pasteur (1822 – 1895). Cuando se encontraba investigando sobre los cristales de tartrato de sodio, pudo observar que algunos compuestos en disolución, desviaban la luz en un sentido y otros, la desviaban en sentido contrario. Louis Pasteur determinó que si los compuestos, en este caso isómeros, presentaban desviación óptica era debido a que sus moléculas tenían una imagen especular, tal como se forma una imagen en un espejo.
Observa el siguiente ejemplo. Ambas imágenes no se pueden superponer, ya que sus lados izquierdo y derecho, son diferentes.
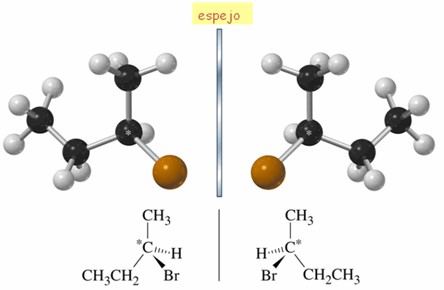
A continuación, revisaremos algunos ejemplos de compuestos químicos, cuyos enantiómeros han impactado de forma positiva o negativa en la industria farmacéutica a nivel mundial.
El enantiómero L de la 3,4–dihidroxifenilalanina o levodopa, actualmente corresponde al medicamento más eficaz contra el tratamiento de la enfermedad de Parkinson. Esta enfermedad se produce por un déficit de dopamina en determinadas áreas del cerebro, lo que ocasiona temblores en las extremidades del cuerpo y se presenta rigidez muscular. Debido a esto, se dificulta la escritura, el habla y el caminar.
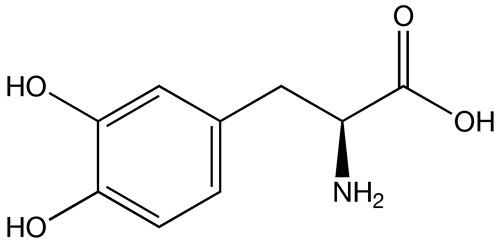
Levodopa
El enantiómero L es el activo y el enantiómero denominado D es inactivo biológicamente. Por lo que, los síntomas de la enfermedad de Parkinson se alivian con el suministro de levodopa, ya que ocasiona un estímulo para aumentar la producción de dopamina.
En estos casos, la dopamina no se puede suministrar directamente al paciente, ya que esta es incapaz de pasar del torrente sanguíneo al cerebro. Es por este motivo, que se administra levodopa, que es el precursor metabólico de la dopamina.
El otro ejemplo, es el ácido 2-(4-isobutilfenil) propiónico más conocido como Ibuprofeno. El Ibuprofeno posee dos formas enantiómeras. La denominada S posee actividad farmacológica, mientras que el enantiómero R no posee actividad antiinflamatoria.
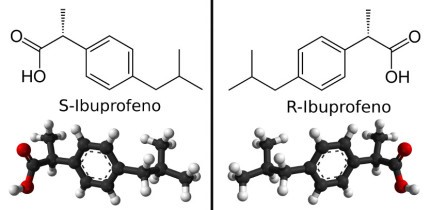
Nuestro cuerpo realiza transformaciones enzimáticas y logra transformar hasta un 60% del enantiómero R en el enantiómero S, que es el activo. Por ejemplo, la dosis más común del Ibuprofeno son 400 mg, la que consiste en una mezcla de sus dos enantiómeros, lo que se conoce como mezcla racémica. Una mezcla racémica posee en igual cantidad ambos enantiómeros de una molécula, en el caso mencionado, 200 mg del enantiómero S y 200 mg del enantiómero R. Por lo que, nuestro cuerpo logra convertir el enantiómero R en activo.
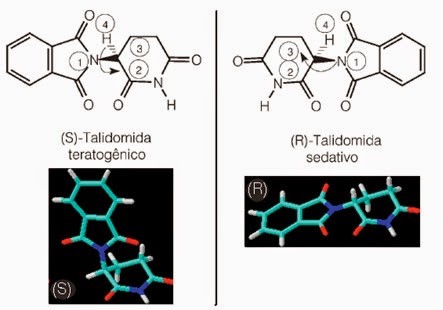
El último ejemplo, corresponde a la talidomida (imida del ácido N-ftalilglutámico). A comienzos de la década de 1960, la producción de medicamentos se vio impactada negativamente por la tragedia de la talidomida.
La talidomida fue suministrada como una mezcla racémica para tratar las náuseas que se producen durante el embarazo. Sin embargo, solo el enantiómero R es el activo, ya que el enantiómero S produce malformaciones en los bebés recién nacidos. Se ha estimado que la talidomida pudo haber afectado a aproximadamente 10 000 niños.
Posteriormente en diversos estudios, se comprobó que el cuerpo humano transforma el enantiómero activo en enantiómero perjudicial, que en este caso corresponde al enantiómero S.